Humuleno

El humuleno, también conocido como α-humuleno o α-cariofileno, es un sesquiterpeno monocíclico natural ( C 15 H 24 ) {\displaystyle {\ce {(C15H24)}}} , que contiene un anillo de once miembros, y está formado por tres unidades de isopreno con tres dobles enlaces C=C no conjugados, dos de ellos sustituidos tres veces y uno sustituido dos veces. Fue encontrado por primera vez en los aceites esenciales de Humulus lupulus (lúpulo), de ahí su nombre. El humuleno es un isómero del β-cariofileno, y ambos se encuentran a menudo juntos en forma de mezcla en muchas plantas aromáticas.
| Humuleno | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| 2,6,6,9-Tetramethyl-1,4-8-cycloundecatriene | ||
| General | ||
| Otros nombres | alpha-Cariofileno; 3,7,10-Humulatrieno | |
| Fórmula estructural |
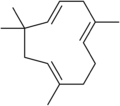 | |
| Fórmula molecular |
C 15H 24 | |
| Identificadores | ||
| Número CAS | 6753-98-6[1] | |
| Número RTECS | GZ4817500 | |
| ChEBI | 5768 | |
| ChEMBL | 251280 | |
| ChemSpider | 4444853 | |
| PubChem | 5281520 | |
| UNII | 54W56MD2WD | |
| KEGG | C09684 | |
|
C\1=C/C(C)(C)C/C=C(/CC/C=C(/C/1)C)C
| ||
| Propiedades físicas | ||
| Apariencia | líquido amarillo verdoso pálido claro | |
| Densidad | 0,886 kg/m³; 0,000886 g/cm³ | |
| Masa molar | 204,35 g/mol | |
| Punto de fusión | 25 °C (298 K) | |
| Punto de ebullición | 106 °C (379 K) | |
| Riesgos | ||
| LD50 | >48 mg/kg | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El humuleno, también conocido como α-humuleno o α-cariofileno, es un sesquiterpeno monocíclico natural , que contiene un anillo de once miembros, y está formado por tres unidades de isopreno con tres dobles enlaces C=C no conjugados, dos de ellos sustituidos tres veces y uno sustituido dos veces.
Fue encontrado por primera vez en los aceites esenciales de Humulus lupulus (lúpulo), de ahí su nombre.[2] El humuleno es un isómero del β-cariofileno, y ambos se encuentran a menudo juntos en forma de mezcla en muchas plantas aromáticas.
Presencia natural
[editar]
El humuleno es uno de los componentes del aceite esencial del cono floral de la planta del lúpulo (Humulus lupulus), de donde deriva su nombre. La concentración de humuleno varía en función de la variedad de planta, pero puede alcanzar hasta el 40 % del aceite esencial. El humuleno y sus productos resultantes del proceso de elaboración de la cerveza son los responsables del aroma «lupulado» de muchas cervezas. Se ha descubierto que las variedades nobles de lúpulo tienen niveles más altos de humuleno, mientras que otras variedades amargas contienen niveles bajos. En el proceso de elaboración de la cerveza se producen múltiples epóxidos de humuleno. En un estudio científico en el que se utilizó cromatografía de gases y espectrometría de masas para analizar muestras y contar con un panel sensorial entrenado, se descubrió que los productos de hidrólisis del epóxido II del humuleno producen específicamente un aroma a «lúpulo» en la cerveza.
El α-humuleno se ha encontrado en muchas plantas aromáticas de todos los continentes, a menudo junto con su isómero, el β-cariofileno. Se ha demostrado que los pinos, los naranjos, los saúcos, el tabaco y los campos de girasoles son emisores de α-humuleno a la atmósfera. El α-humuleno está presente en los aceites esenciales de plantas aromáticas como la Salvia officinalis (salvia común o salvia culinaria), Lindera aggregata (uyaku o arbusto de especias japonés), especies de ginseng, hasta un 29,9 % de los aceites esenciales de Mentha spicata, la familia del jengibre (Zingiberaceae), el 10 % del aceite de las hojas de Litsea mushaensis (un laurel chino), el 4 % del extracto de las hojas de Cordia verbenacea (erva baleeira), pero con un 25 % de trans-cariofileno y es uno de los compuestos químicos que contribuyen al sabor de la especia pimienta de Sichuan.También está presente en P. odorata o cilantro vietnamita y en el aroma característico del cannabis.[3]
Preparación y síntesis
[editar]El humuleno es uno de los muchos sesquiterpenoides derivados del difosfato de farnesilo (FPP). La formación de humuleno a partir del FPP está catalizada por enzimas de síntesis de sesquiterpenos.[4]

Este proceso puede imitarse en el laboratorio mediante la preparación de estannano alílico a partir de farnesol, lo que se conoce como síntesis de Corey.
Existen diversas formas de sintetizar humuleno en el laboratorio que implican diferentes cierres del enlace C-C en el macrocíclo. La síntesis de McMurry emplea una reacción de acoplamiento de carbonilo catalizada por titanio, la síntesis de Takahashi utiliza la alquilación intramolecular de un haluro de alilo por un anión cianohidrina protegido, la síntesis de Suginome emplea un fragmento de geranilo y la síntesis de de Groot sintetiza humuleno a partir de un destilado crudo de aceite de eucalipto.[5]
El humuleno también se puede sintetizar mediante una combinación de ensamblaje de cuatro componentes y ciclación mediada por paladio, que se describe a continuación. Esta síntesis es notable por la simplicidad con la que se forman los enlaces C-C y los pasos de ciclación, lo que se cree que resultará ventajoso en la síntesis de politerpenoides relacionados.[6]
Para comprender la regioselectividad del humuleno, el hecho de que uno de los dos dobles enlaces C═C triplemente sustituidos sea significativamente más reactivo, se exploró computacionalmente su espacio conformacional y se identificaron cuatro conformaciones diferentes.[7]
Investigación
[editar]En estudios de laboratorio, se está investigando el humuleno por sus posibles efectos antiinflamatorios.[8][9] En 2015, investigadores de Brasil identificaron el α-humuleno como un contribuyente activo a las propiedades repelentes de insectos del aceite de hoja de Commiphora leptophloeos, específicamente contra el «mosquito de la fiebre amarilla», Aedes aegypti.[10]
Química atmosférica
[editar]El α-humuleno es un compuesto orgánico volátil biogénico que se emite por numerosas plantas (véase «Presencia») y tiene un potencial relativamente alto para formar aerosoles orgánicos secundarios en la atmósfera.
Reacciona rápidamente con el ozono en presencia de luz solar (fotooxidación) para formar productos oxigenados. El coeficiente de velocidad de reacción en la reacción bimolecular del α-humuleno es muy alto ((1.17 × 10−14 cm3 molécula−1 s−1) en comparación con el de la mayoría de los monoterpenos.
Al tener tres dobles enlaces, pueden formarse productos de primera, segunda y tercera generación, que pueden condensarse para formar aerosoles orgánicos secundarios. Con unas proporciones de mezcla de ozono troposférico típicas de 30 partes por billón, la vida útil del α-humuleno es de aproximadamente dos minutos, mientras que los productos de primera y segunda generación tienen una vida media de una hora y doce horas, respectivamente.[11]
Referencias
[editar]- ↑ Número CAS
- ↑ «Hop Aroma and Flavor». realbeer.com. Consultado el 13 de febrero de 2026.
- ↑ «Beer Breakthrough: Hops May Prevent Pasture-Associated Laminitis». Horse Collaborative. 1 de agosto de 2014. Archivado desde el original el 7 de diciembre de 2014. Consultado el 11 de diciembre de 2014.
- ↑ «humulene biosynthesis». www.enzyme-database.org. Consultado el 13 de febrero de 2026.
- ↑ Goldsmith, David. "The total synthesis of natural products". Canada: John Wiley & Sons. 1997 pp 129-133
- ↑ Hu, Tao & E. J. Corey (2002). «Short Syntheses of (±)-δ-Araneosene and Humulene Utilizing a Combination of Four-Component Assembly and Palladium-Mediated Cyclization». Organic Letters 4 (14): 2441-2443. PMID 12098267. doi:10.1021/ol026205p.
- ↑ Neuenschwander, U et al. (2012). «Origin of Regioselectivity in α-Humulene Functionalization». J. Org. Chem 77 (6): 2865-2869. doi:10.1021/jo3000942.
- ↑ Passosa, G.F.; Fernandesa, ES. (2007). «Anti-inflammatory and anti-allergic properties of the essential oil and active compounds from Cordia verbenacea». Journal of Ethnopharmacology 110 (2): 323-333. PMID 17084568. doi:10.1016/j.jep.2006.09.032.
- ↑ Fernandes E.S.; Passos G.F.; Medeiros R.; da Cunha F.M.; Ferreira J.; Campos M.M.; Pianowski L.F.; Calixto J.B. (2007). «Anti-inflammatory effects of compounds alpha-humulene and (−)-trans-caryophyllene isolated from the essential oil of Cordia verbenacea». European Journal of Pharmacology 569 (3): 228-236. PMID 17559833. doi:10.1016/j.ejphar.2007.04.059.
- ↑ Santos da Silva, R.C.; Milet-Pinheiro, P.; Bezerra da Silva, P.C.; Gomes da Silva, A.; Vanusa da Silva, M.; Amaral Ferraz Navarro, D.M.; da Silva, N.H. (19 de diciembre de 2015). «(E)-Caryophyllene and α-Humulene: Aedes aegypti Oviposition Deterrents Elucidated by Gas Chromatography-Electrophysiological Assay of Commiphora leptophloeos Leaf Oil». En Boudko, Dmitri, ed. PLOS ONE 10 (12). Bibcode:2015PLoSO..1044586D. PMC 4674132. PMID 26650757. doi:10.1371/journal.pone.0144586.
- ↑ Beck, M.; Winterhalter, R.; Herrmanna, F.; Moortgat, G. K. (2011). «The gas-phase ozonolysis of α-humulene». Phys. Chem. Chem. Phys. 13 (23): 10970-11001. Bibcode:2011PCCP...1310970B. PMID 21461420. doi:10.1039/c0cp02379e.
Enlaces externos
[editar]- Esta obra contiene una traducción derivada de «Humulene» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
![{\displaystyle {(\mathrm {C} {\vphantom {A}}_{\smash[{t}]{15}}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{24}})}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9120c13d3776aced689b9412a0ed2e2592d87ac3)
